Uniones Químicas
Espacio Curricular: Química.
Docente: Tassin, Maria Laura.
Tema: UNIONES QUÍMICASENLACES QUÍMICOS.
A. INICIO
Vamos a incorporar un poquito más, utilizando todos
los conceptos vistos en las secuencias anteriores.
¿¿¿Vamos???
Conocimientos:
-
Enlaces químicos:
-
Teoría del octeto.
-
Notación de Lewis.
-
Enlaces covalentes (simple, dobles, triples)
-
Propiedades.
-
Formación de aniones y cationes.
Objetivos:
- - Relacionar las características del enlace
iónico, covalente y metálico con las propiedades macroscópicas de los
compuestos.
- - Demostrar un pensamiento crítico y
reflexionar sobre lo aprendido.
¿CÓMO
SE FORMA LA MATERIA?
TIPOS
DE ENLACES QUÍMICOS, EJEMPLOS Y CARACTERÍSTICAS
El agua, el aire, las rocas y hasta nosotros mismos
estamos compuestos de átomos. Normalmente estas unidades básicas de la materia
no vagan por el espacio en soledad, sino que se combinan con otros átomos e
interactúan con ellos gracias a los enlaces químicos.
Entender qué son los enlaces químicos nos
ayudará a comprender mejor las propiedades de la materia y las reacciones
químicas, responsables de cambios
químicos que ves en tu día a día.
¿QUÉ SON LOS ENLACES
QUÍMICOS?
Llamamos enlace químico a la fuerza por la que los
átomos de un compuesto se mantienen unidos. Se trata de fuerzas
electromagnéticas que, como te explicaremos a continuación, dan lugar a
diferentes tipos de enlaces químicos.
¿Por qué se forma un enlace químico?
Para saber cómo se forman enlaces químicos, primero
tienes que entender qué es un átomo y cómo se comporta.
Repasemos:
Un átomo está formado por un núcleo rodeado de electrones, que tienen
carga negativa. Al tener cargas opuestas, estas dos partes del átomo se atraen
entre ellas. Sin embargo, por esta misma razón los electrones también se ven
atraídos hacia los núcleos de otros átomos.
REGLA
DEL OCTETO
Los átomos tienden a formar enlaces químicos porque
cuando se unen a otros átomos alcanzan una situación más estable, es decir, la
que les supone un consumo de energía menor. Esto ocurre cuando el número de
electrones de su último nivel es igual a ocho, lo que se conoce como la regla
del octeto. Es cierto que no es una norma que se pueda aplicar a todos los
átomos, pero sí a la mayoría.
Para cumplir con la regla del octeto, los átomos
pueden ceder electrones, ganarlos o incluso compartirlos con otro átomo. Como
resultado, se obtienen varios tipos de enlaces químicos distintos.
TIPOS DE ENLACES
Como dijimos al principio,
el hecho de que los átomos se combinen o enlacen para formar nuevas sustancias
se explica por la tendencia a conformar estructuras más estables. De ahí que
dichos enlaces químicos sean considerados como un incremento de estabilidad.
Para lograr ese estado
ideal estable, los átomos pueden utilizar algún método que les acomode,
eligiendo entre: ceder o captar electrones, compartir electrones con otro átomo
o ponerlos en común junto con otros muchos.
De estas tres posibilidades
nacen los tres tipos de enlace químico:
-
Enlace iónico.
-
Enlace Covalente.
-
Enlace Metálico.
Tomando como base la Diferencia
de Electronegatividad entre los átomos que forman un enlace se puede predecir
el tipo de enlace que se formará:
|
Si la diferencia de electronegatividades es mayor que 2. |
= |
se formará un Enlace iónico |
|
Si la diferencia de electronegatividades es mayor que 0,5 y menor a
2,0. |
= |
el enlace formado será Covalente polar |
|
Si la diferencia de electronegatividades es menor a 0,5 o igual a 0 |
= |
el enlace será Covalente puro (o no polar). |
Un acaso particular es el
enlace covalente coordinado:
Se establece por
compartición de electrones entre dos átomos, pero sólo un átomo aporta el par
de electrones compartidos.
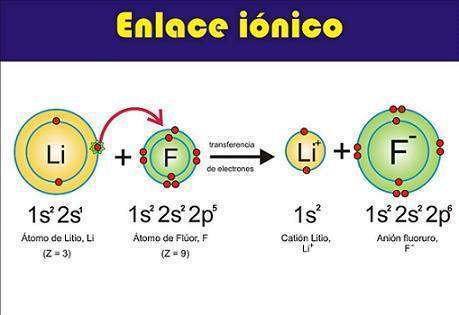
ENLACE IÓNICO
El enlace
iónico se forma cuando existe transferencia de electrones, este tipo de enlace
se da por ejemplo cuando se forma una molécula a partir de la unión de un metal
con un no metal. La ganancia o pérdida de electrones se produce para que
los átomos alcancen la configuración de los gases nobles en su último nivel (ns2np6),
esto les confiere estabilidad, quedando en forma de iones. Los átomos que
ceden su electrón, quedan con carga positiva y se denominan cationes, y los
átomos que ganan electrones quedan con carga negativa y se denominan aniones.
Entonces, los iones de diferentes signos se atraen electrostáticamente,
formando enlaces iónicos, donde se unen un catión (átomo que cede su electrón)
con un anión (átomo que capta un electrón).
El enlace
iónico se produce cuando se unen dos átomos cuyas diferencias de
electronegatividad son importantes ΔEN › 2,0, otra manera de
reconocer la presencia de enlace iónico es que éste se produce cuando se unen
elementos del grupo I y II A con elementos del grupo VI y VII A.
Un ejemplo de
este enlace iónico se muestra a continuación: molécula de Cloruro de Sodio NaCl
(sal común), el sodio (Na) pertenece al grupo IA y el cloro (Cl) pertenece al
grupo VIIA, la diferencia de electronegatividad de estos elementos es ΔEN
= 2,1. El sodio es un metal alcalino y el cloro un no metal perteneciente
a la familia de los halógenos.
a
PROPIEDADES DEL ENLACE IÓNICO
Los productos
resultantes de un enlace iónico poseen características especiales:
- Son enlaces fuertes. La fuerza de esta unión
atómica puede ser muy intensa, por lo que la estructura de estos compuestos
tiende a formar redes cristalinas muy resistentes.
-
Suelen ser sólidos. A temperaturas y rangos de presión normales (T=25ºC y P=1atm),
estos compuestos tienen estructura molecular cúbica y rígida, que forma redes
cristalinas que originan sales. También existen líquidos iónicos denominados
“sales derretidas”, que son poco frecuentes, pero sumamente útiles.
-
Poseen un alto punto de
fusión y ebullición. Tanto el punto de fusión (entre 300 ºC y 1000
ºC) como el de ebullición de estos compuestos suele ser muy alto,
pues se requieren grandes cantidades de energía para romper la atracción
electrostática entre los iones.
-
Solubilidad en agua. La mayoría de las sales son solubles en agua y otras soluciones acuosas
que presenten un dipolo eléctrico (polos positivo y negativo).
-
Conducción eléctrica. En su estado sólido no son buenos conductores
de electricidad, dado que los iones ocupan posiciones muy fijas en una red
cristalina. En cambio, una vez disueltos en agua o en solución acuosa, se
tornan eficaces conductores de la electricidad.
- Selectividad. Los enlaces iónicos pueden darse únicamente
entre metales de los grupos IA y IIA de la Tabla Periódica, y los no
metales de los grupos VIA y VIIA. - Fuente: https://concepto.de/enlace-ionico/
ENLACE COVALENTE
En el enlace covalente los
átomos comparten electrones para lograr la configuración
electrónica de gas noble y por lo tanto tener estabilidad similar a estos. Este
tipo de enlace está asociado al concepto planteado por Lewis, que indica que
los átomos deben completar un octeto (8 electrones a su alrededor) cuando se
une a otros a través del enlace covalente, la excepción es el átomo de
Hidrógeno que sólo se rodea de dos electrones cuando establece enlace covalente
ya sea con otro átomo de hidrógeno para formar la molécula de hidrógeno, H2 o
bien con otros átomos. Otros átomos.
A continuación se describe
la formación de un enlace químico en el hidrógeno (H2) como: cada
átomo de hidrógeno a porta con un electrón H• •H , cuando dos átomos
comparten un par de electrones, estos se representan como una línea en la estructura
de Lewis: H−H
Para determinar la
formación del enlace covalente se puede determinar la diferencia de
electronegatividad de una molécula diatómica:
-Si ΔEN <2,0,
entonces es un enlace covalente que se define particularmente como enlace
covalente polar , y
-Si la ΔEN =0,
entonces se trata de un enlace covalente apolar, este enlace se da en las
moléculas diatómicas simétricas, es decir, formadas por el mismo tipo de
átomos, ejemplos: H2, O2, Cl2, etc.
Conceptos
importantes a considerar:
- En los enlaces covalentes entre átomos poli
electrónicos (muchos e-) sólo participan los electrones de valencia (n°
del grupo).
- Concepto de estructura de Lewis→
regla del octeto (rodearse de 8 electrones)
- La
diferencia de electronegatividad entre los átomos es pequeña comparada con
la de los enlaces iónicos.
ENLACE COVALENTE APOLAR
Si los átomos enlazados son no metales e idénticos (como en N2 o
en O2), los electrones son compartidos por igual por los dos átomos,
y el enlace se llama covalente apolar.
Se establece entre átomos con igual electronegatividad. Átomos
del mismo elemento presentan este tipo de enlace.
Enlace covalente Apolar: Molécula de N2 (Notación
de lewis)
a
En este enlace covalente no polar, la densidad electrónica es
simétrica con respecto a un plano perpendicular a la línea entre los dos
núcleos. Esto es cierto para todas las moléculas diatómicas homonucleares
(formadas por dos átomos del mismo elemento), tales como H2, O2,
N2, F2 y Cl2, porque los dos átomos
idénticos tienen electronegatividades idénticas. Por lo que podemos
decir: los enlaces covalentes en todas las moléculas diatómicas
homonucleares deben ser no polares.
ENLACE COVALENTE POLAR
Si los átomos son no metales, pero distintos (como en el óxido nítrico,
NO), los electrones son compartidos en forma desigual y el enlace se llama
covalente polar (polar porque la molécula tiene un polo eléctrico positivo y
otro negativo, y covalente porque los átomos comparten los electrones, aunque
sea en forma desigual).
Se establece entre átomos
con electronegatividades próximas, pero no iguales.
Estas sustancias no
conducen la electricidad ni tienen brillo, ductilidad o maleabilidad.
Por lo tanto, el enlace será covalente
polar, aunque, si no se conociera la electronegatividad de los elementos
bastaría saber que son dos no metales distintos para definir su enlace como
covalente polar.
PROPIEDADES DE LOS ENLACES COVALENTES
• Son gases, líquidos o sólidos de bajo punto de fusión.
• La
mayoría son insolubles en disolventes polares.
• La
mayoría son solubles en disolventes apolares.
• Los
líquidos y sólidos fundidos no conducen la electricidad.
• Las
disoluciones acuosas son malas conductoras de la electricidad porque no
contienen partículas cargadas
ENLACE METALICO
Si los átomos enlazados son
elementos metálicos, el enlace se llama metálico. Los electrones
son compartidos por los átomos, pero pueden moverse a través del sólido proporcionando
conductividad térmica y eléctrica, brillo, maleabilidad y ductilidad. Los
electrones que participan en él se mueven libremente, a causa de la poca fuerza
de atracción del núcleo sobre los electrones de su periferia.
Cuando los electrones son
compartidos simétricamente, el enlace puede ser metálico o covalente apolar; si
son compartidos asimétricamente, el enlace es covalente polar; la transferencia
de electrones proporciona enlace iónico. Generalmente, la tendencia a una distribución
desigual de los electrones entre un par de átomos aumenta cuanto más separados
están en la tabla periódica.
RESUMEN:
ENLACES QUÍMICOS ENTRE MOLÉCULAS
Hasta el momento hemos visto los principales
enlaces químicos entre átomos. Sin embargo, también nos podemos
encontrar con otros enlaces químicos entre moléculas. Estos se
consideran enlaces temporales, ya que son más débiles. Aun así, son esenciales
para la vida porque son los que mantienen unidas a las moléculas. Sin ellos,
las encontraríamos dispersas por el ambiente. Es decir, no existiría el estado
líquido ni el estado sólido, solo el gaseoso.
A continuación, te mostramos algunos ejemplos
de enlaces químicos entre moléculas:
- Puente
de hidrógeno
Los enlaces de hidrógeno ocurren cuando el
hidrógeno interactúa con otro elemento de alta polaridad. En estos casos, el
hidrógeno tiene carga positiva, razón por la cual es atraído hacia los átomos
con carga negativa, creando un puente de hidrógeno con ellos.
Aunque este tipo de enlace químico es débil, es muy
común. Por ejemplo, son muy habituales los puentes de hidrógeno del agua.
- Fuerzas
de dispersión de London
En el caso de las fuerzas de dispersión de
London, la unión se puede dar entre cualquier tipo de molécula. Se trata
también de enlaces débiles, debidos a desequilibrios temporales en la
distribución de los electrones.
Como ya hemos comentado, los electrones siempre
están moviéndose por el espacio. Por esta razón, hay momentos en los que se
agrupan, creando una carga negativa en una parte de la molécula y una positiva
en la otra. Si esta molécula está cerca de otra molécula en la que las cargas
eléctricas están desequilibradas, sus cargas opuestas se atraerán entre sí.
A continuación, un gráfico que resume todas las
posibilidades de interacciones entre moléculas:
¿POR QUÉ ES IMPORTANTE CONOCER LOS TIPOS DE ENLACES QUÍMICOS?
Ya has visto que los átomos y las moléculas
interactúan entre sí de diferentes modos y esto influye en las propiedades de
los compuestos químicos que se generan. Conocer los diferentes tipos de enlaces
químicos nos ayuda a entender mejor el mundo y a darnos cuenta de que la
química tiene un papel indispensable en nuestra vida.
C. CIERRE
Bueno chicos como vimos anteriormente este tema es
más específico de la Química, y debemos tener todos los conocimientos
anteriores en nuestra mente como la evolución de los átomos, la estructura
atómica de los elementos químicos, configuración electrónica, números
cuánticos, además necesitamos tener muy presente el uso adecuado de la tabla
periódica.
D. AUTOEVALUACION
A continuación, vamos a realizar una pequeña
autoevaluación para que puedas comprobar tú mismo tus conocimientos previos.
a.
¿Cuál fue el tema que más
te llamó la atención?
b.
¿Qué tema consideras que
conocías de antes?
c.
Los saberes desarrollados
con anterioridad, los entiendes (Marcar con una cruz):
§ Muy bien.
§ Bien.
§ Poco
§ Casi nada.
d.
¿Te quedaron dudas o
preguntas que te gustaría debatir con el profesor? ¿Cuáles?
e.
¿Pensas que aprendiste algo
nuevo?
BIBLIOGRAFIA:
-
https://concepto.de/enlace-ionico/
-
http://www.aulatecnologica.cl/rdi/quimica/clase(1)/clase1/enlace_covalente_apolar.html

Comentarios
Publicar un comentario